オンラインカジノ Actuate Therapeutics社、ASCO2025年次総会でエラグルシブ第2相試験のトップラインデータを発表:転移性膵癌のファーストライン治療において、主要評価項目である全生存期間中央値を達成し、1年生存期間を2倍に延長
Page Info
View照会: 177
登録日: 25-06-01 08:00
本文
第2相試験(Actuate-1801 Part 3B)において、主要評価項目を達成し、elraglusib/GnPを投与された前治療歴のない転移性膵管腺癌(mPDAC)患者において、臨床的に意義のある全生存期間中央値の延長(10.1カ月 vs 7.2カ月、log-rank p=0.01)が示される
死亡リスクはエルラグルシブ/GnP投与群で37%減少した(HR=0.63)。
データはASCO年次総会で口頭発表された。
2025年後半にFDAと協働し、製品登録への道筋をつける予定
本日午後6時30分(米国東部標準時間)よりKOLイベントを開催し、1801パート3Bの結果について説明する。
2025年5月31日、シカゴおよびテキサス州フォートワース(GLOBE NEWSWIRE) -- Actuate Therapeutics, Inc.(NASDAQ:ACTU)(以下「アクチュエイト」または「当社」)は、グリコーゲン合成酵素キナーゼ-3ベータ(GSK-3β)の阻害による影響が大きく治療が困難ながんの治療法の開発に注力する臨床段階のバイオ医薬品企業です、本日、米国臨床腫瘍学会(ASCO)年次総会において、前治療歴のない転移性膵管腺癌(mPDAC)患者を対象としたゲムシタビン/ナブパクリタキセル(GnP)併用療法におけるエルラグルシブの第2相試験(Actuate-1801 Part 3B)のトップライン結果を発表しました。
抄録タイトル未治療の転移性膵管腺癌(mPDAC)患者を対象としたエルラグルシブとゲムシタビン/ナブパクリタキセル(GnP)併用療法とGnP単独療法の無作為化第2相試験(1801パート3B)の予備的結果。
抄録番号:4006
セッションタイトル消化器癌-胃食道癌、膵癌、肝胆膵癌
発表者Devalingam Mahalingam医学博士
口頭発表日時:2025年5月31日(土)4:48 PM CDT
本試験は主要評価項目である全生存期間中央値の改善を達成した。全生存期間(mOS)中央値は、死亡リスクを37%減少させ、強い統計学的有意性を伴ってほぼ3ヵ月延長し(10.1ヵ月 vs 7.2ヵ月、HR=0.63、log-rank p=0.01)、mPDACの潜在的治療において臨床的に意義のある前進を示した。エルラグルシブとGnPの併用療法を受けた患者の12ヵ月生存率は44.1%で、GnP単独療法(22.3%)の2倍であった。
ノースウェスタン大学ファインバーグ医学部のDeva Mahalingam医師(PhD)は、1801パート3B試験の治験責任医師であり、次のようにコメントしている。「膵臓がんは、近年、一部の患者におけるいくつかの分子標的を除いては、大きな治療法の進歩がなく、依然として最もアンメット・メディカル・ニーズの高いがんの1つです。新たな作用機序が早急に必要とされています。ゲムシタビンとナブパクリタキセルという既存の化学療法のバックボーンにエルラグルシブを加えることは有望であり、膵臓がん患者にとって意味のある治療の進歩になる可能性があります。"と述べている。
アクチュエイト社のダニエル・シュミット社長兼最高経営責任者(CEO)は、「mOSを大幅に改善し、死亡リスクを37%低減し、12ヶ月生存率を2倍にしました。管理可能な安全性プロファイルと、新たに明らかになった強力なメカニズム的洞察と相まって、これらの結果は、当社のGSK-3β阻害剤プログラムの変革の可能性を補強するものです。明確な臨床的有用性と忍容性の高い安全性プロファイルに基づき、我々は今年後半にFDAおよびEMAと交渉し、登録への道筋をつけるつもりである。これにより、このファースト・イン・クラスの治療薬を商業化し、緊急のアンメット・ニーズを抱える患者さんに提供できるよう、迅速に進めることができると考えています」。
有効性
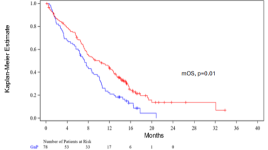
以下の図1は、mOSのカプラン・マイヤー推定値(10.1カ月 vs 7.2カ月、HR=0.63、log-rank p=0.01)を示しており、死亡リスクが37%減少していることから、エルラグルシブ/GnP併用療法群とGnP単独療法群との比較において、エルラグルシブ/GnP併用療法群で治療を受けた患者に明らかな臨床的生存ベネフィットがあることを示している。
図1:Actuate-1801 Part 3B:2025年3月27日時点のmOSのカプランマイヤー推定値(トップラインデータカットオフ)。
mOSおよび1年生存率の改善に加えて、18ヵ月後および24ヵ月後においても生存の継続的なベネフィットが観察された(生存率はそれぞれ、エルラグルシブ/GnP併用群対GnP群で19.7%対4.4%、13.8%対0%)。
また、エルラグルシブ/GnP併用療法では、全奏効率が数値的に改善し(エルラグルシブ/GnP併用療法群29.0%対GnP併用療法群21.8%)、無増悪生存期間中央値および奏効期間中央値は、それぞれエルラグルシブ/GnP併用療法群5.6カ月対5.1カ月、エルラグルシブ/GnP併用療法群5.5カ月対GnP併用療法群4.0カ月と改善した。
安全性およびバイオマーカー所見
本試験は主要安全性エンドポイントも達成した。エルラグルシブ/GnP併用群における治療有害事象(TEAE)および重篤な有害事象(SAE)はGnP併用群で観察されたものと同様であり、エルラグルシブ/GnP併用群の良好なリスク・ベネフィット・プロファイルを示した。
治療関連有害事象(TRAE)はほとんどがグレード1~2であり、最も頻繁に観察されたTRAE(患者の約3分の2)は一過性の視覚障害で、可逆的かつ非進行性であった。
グレード3以上の好中球減少症が観察された一方で、発熱性好中球減少症および敗血症の発生率は両群で同程度であった。
投与前のサイトカイン解析では、CCL3、IL-1α、IL-18、TGF-β、TRAIL R3などの主要な免疫調節因子のベースライン値が低いことが示唆され、1年生存率の改善と相関していた。
CD8陽性およびグランザイムB陽性T細胞の増加、NK細胞の増加、および骨髄由来抑制細胞の減少が、エルラグルシブ治療患者の腫瘍生検でのみ観察された。この探索的な結果は、mPDAC患者においてエラグルシブが提唱する免疫調節作用の機序を裏付けるものである。
KOLイベント
アクチュエイト社は、本日2025年5月31日午後6時30分(米国東部標準時間)より、投資コミュニティー向けにKOLイベントを開催し、本データをレビューします。このウェビナーでは、アクチュエイトの社長兼最高経営責任者(CEO)ダニエル・シュミットが司会を務め、4人の著名なKOLが参加します:メイヨークリニック医科科学大学Tanios Bekaii-Saab医学博士(FACP)、ノースウェスタン大学ファインバーグ医学部Devalingam Mahalingam医学博士、アリゾナ大学がんセンターRachna Shroff医学博士、アリゾナ大学がんセンターMS、FASCO、マサチューセッツ総合病院Colin Weekes医学博士。
イベントの詳細
日時:2025年5月31日(土)午後6時30分(米国東部標準時
形式 対面およびライブ・ウェブキャスト
登録: こちらをクリック
当日の模様は、アクチュエイトのウェブサイトの投資家向け情報セクションでご覧いただけます。
Actuate-1801 Part 3B Studyについて
Actuate-1801 Part 3B試験(NCT03678883)は、mPDACの一次治療におけるエルラグルシブとGnPの併用療法とGnP単独療法の無作為化比較第2相試験です。本試験には、転移性疾患に対する全身治療歴のないmPDAC患者286人が登録され、エルラグルシブ治療群(エルラグルシブ+GnP)と対照群(GnP単独)に2:1で無作為に割り付けられた。エルラグルシブは9.3mg/kgの用量で、28日サイクルの各週の1日目に点滴静注される。本試験の主要評価項目は全生存期間中央値であり、OSは本試験全体を通して1年生存期間の推定値で要約される。副次評価項目はDCR、ORR、PFS、AEである。
GSK-3βの阻害は、化学療法活性の増強、自然抗腫瘍免疫の活性化、遺伝子発現の調節、腫瘍代謝の変化や上皮間葉転換(EMT)をもたらすなど、いくつかの相補的な機序によって腫瘍の増殖を抑制し、生存率を改善する可能性がある。
アクチュエイト・セラピューティクス社について
アクチュエイト社は、影響が大きく治療が困難な癌の治療法の開発に重点を置く臨床段階のバイオ医薬品企業である。アクチュエイト社の主要な治験薬であるエルラグルシブ(新規GSK-3β阻害剤)は、活性化B細胞のκ-光鎖-エンハンサー核因子(NF-kB)およびDNA損傷応答(DDR)を阻害することにより、腫瘍の成長を促進し、化学療法などの従来の抗癌剤に対する抵抗性に関与する癌の分子経路を標的とする。エラグルシブはまた、複数の免疫チェックポイントと免疫細胞の機能を制御することにより、抗腫瘍免疫を仲介する可能性がある。追加情報については、当社ウェブサイトhttp://www.actuatetherapeutics.com。
将来の見通しに関する記述
本プレスリリースには、当社およびその他の関係者の臨床試験および開発計画、ならびに当社業界に関する将来の見通しに関する記述が含まれています。予想する」、「信じる」、「継続する」、「可能性がある」、「推定する」、「期待する」、「意図する」、「可能性がある」、「かもしれない」、「進行中である」、「計画する」、「可能性がある」、「予測する」、「プロジェクトする」、「はずである」、「目標する」、「する予定である」、「だろう」、またはこれらの用語の否定形、あるいはその他の同等の用語は、将来見通しに関する記述を識別することを意図していますが、すべての将来見通しに関する記述がこれらの識別語を含んでいるわけではありません。本プレスリリースに含まれる、現在の事実もしくは現在の状況または過去の事実に関連する記述を除くすべての記述は、将来の見通しに関する記述です。従って、これらの記述には見積もり、仮定、重大なリスクおよび不確実性が含まれており、実際の結果が記述に示されたものと大きく異なる可能性があります。予備的データおよび未発表データは、より多くのデータが入手可能になった後、またはデータをより包括的に検討した後に変更され、さらに解釈される可能性があり、最終的な分析として依拠すべきではありません;臨床試験データが、規制当局や医学界で異なる解釈や評価の対象となるリスク、臨床および前臨床の医薬品開発には、タイムラインや結果が不確実な、長期的で費用のかかるプロセスが含まれること、先行する前臨床試験や初期の臨床試験の結果は必ずしも将来の結果を予測するものではなく、エラグルシブが良好な臨床結果や良好な前臨床試験結果を達成できない可能性があること、また、規制当局への申請や承認取得を適時に行うことができない可能性があること;FDAまたはEMAとの対話およびそのような機関が課す可能性のある開発基準を含め、さらなる患者の追加登録に成功しない、またはさらなる開発計画を確立または前進させることができない可能性があること、エラグルシブに副作用、有害事象、その他の特性または安全性リスクが伴う可能性があり、その結果、規制当局の承認が遅延または妨げられる可能性があること、臨床試験を中断または中止させる可能性があること、その他の否定的な結果をもたらす可能性があること、非臨床試験および臨床試験を実施するために第三者に依存していること、第三者のライセンサーに依存していること、および当社の知的財産権を維持し保護する能力があること;当社が他のバイオテクノロジー企業や製薬企業との大きな競争に直面していること、当社の財務状況により継続企業の前提に重要な疑義が生じ、2025年度第2四半期以降の事業資金を調達するために追加資本を必要としていることを含め、当社の開発活動資金調達能力、この必要な資本を短期間に許容可能な条件で、または全く調達できない場合、当社は開発プログラム、商業化努力またはその他の事業の遅延、制限、縮小または終了を余儀なくされる可能性があります。さらに、将来の見通しに関する記述は、「項目1A.2025年3月13日にSECに提出された2024年12月31日終了年度の年次報告書(フォーム10-K)、2025年5月15日にSECに提出された2025年3月31日終了四半期の四半期報告書(フォーム10-Q)、およびSECへのその他の提出書類に記載されている「リスク要因」の見出しを参照することにより、将来の見通しに関する記述の全体が制限されます。上記のリスク要因により、実際の結果や業績が、当社または当社のために作成された将来見通しに関する記述で表明されたものと大きく異なる可能性があるため、将来見通しに関する記述を過度に信頼すべきではありません。さらに、いかなる将来予想に関する記述も、それが作成された時点のものでしかありません。新たな要因は随時発生するものであり、どの要因が発生するかを予測することは不可能です。加えて、各要因が当社の事業に与える影響や、各要因または各要因の組み合わせによって実際の結果が将来の見通しに関する記述に含まれるものとどの程度異なるかを評価することはできません。法的に義務付けられている場合を除き、当社は、本プレスリリースの日付以降の事象や状況を反映したり、予期せぬ事象の発生を反映したりするために、そのような将来見通しに関する記述の修正を公表する義務を負うものではありません。
投資家連絡先
マイク・モイヤー
マネージング・ディレクター
ライフサイ・アドバイザーズLLC
mmoyer@lifesciadvisors.com
この発表に添付された写真は https://www.globenewswire.com/NewsRoom/AttachmentNg/ec493cba-bb28-4bc9-adae-263985865ae6 でご覧いただけます。
死亡リスクはエルラグルシブ/GnP投与群で37%減少した(HR=0.63)。
データはASCO年次総会で口頭発表された。
2025年後半にFDAと協働し、製品登録への道筋をつける予定
本日午後6時30分(米国東部標準時間)よりKOLイベントを開催し、1801パート3Bの結果について説明する。
2025年5月31日、シカゴおよびテキサス州フォートワース(GLOBE NEWSWIRE) -- Actuate Therapeutics, Inc.(NASDAQ:ACTU)(以下「アクチュエイト」または「当社」)は、グリコーゲン合成酵素キナーゼ-3ベータ(GSK-3β)の阻害による影響が大きく治療が困難ながんの治療法の開発に注力する臨床段階のバイオ医薬品企業です、本日、米国臨床腫瘍学会(ASCO)年次総会において、前治療歴のない転移性膵管腺癌(mPDAC)患者を対象としたゲムシタビン/ナブパクリタキセル(GnP)併用療法におけるエルラグルシブの第2相試験(Actuate-1801 Part 3B)のトップライン結果を発表しました。
抄録タイトル未治療の転移性膵管腺癌(mPDAC)患者を対象としたエルラグルシブとゲムシタビン/ナブパクリタキセル(GnP)併用療法とGnP単独療法の無作為化第2相試験(1801パート3B)の予備的結果。
抄録番号:4006
セッションタイトル消化器癌-胃食道癌、膵癌、肝胆膵癌
発表者Devalingam Mahalingam医学博士
口頭発表日時:2025年5月31日(土)4:48 PM CDT
本試験は主要評価項目である全生存期間中央値の改善を達成した。全生存期間(mOS)中央値は、死亡リスクを37%減少させ、強い統計学的有意性を伴ってほぼ3ヵ月延長し(10.1ヵ月 vs 7.2ヵ月、HR=0.63、log-rank p=0.01)、mPDACの潜在的治療において臨床的に意義のある前進を示した。エルラグルシブとGnPの併用療法を受けた患者の12ヵ月生存率は44.1%で、GnP単独療法(22.3%)の2倍であった。
ノースウェスタン大学ファインバーグ医学部のDeva Mahalingam医師(PhD)は、1801パート3B試験の治験責任医師であり、次のようにコメントしている。「膵臓がんは、近年、一部の患者におけるいくつかの分子標的を除いては、大きな治療法の進歩がなく、依然として最もアンメット・メディカル・ニーズの高いがんの1つです。新たな作用機序が早急に必要とされています。ゲムシタビンとナブパクリタキセルという既存の化学療法のバックボーンにエルラグルシブを加えることは有望であり、膵臓がん患者にとって意味のある治療の進歩になる可能性があります。"と述べている。
アクチュエイト社のダニエル・シュミット社長兼最高経営責任者(CEO)は、「mOSを大幅に改善し、死亡リスクを37%低減し、12ヶ月生存率を2倍にしました。管理可能な安全性プロファイルと、新たに明らかになった強力なメカニズム的洞察と相まって、これらの結果は、当社のGSK-3β阻害剤プログラムの変革の可能性を補強するものです。明確な臨床的有用性と忍容性の高い安全性プロファイルに基づき、我々は今年後半にFDAおよびEMAと交渉し、登録への道筋をつけるつもりである。これにより、このファースト・イン・クラスの治療薬を商業化し、緊急のアンメット・ニーズを抱える患者さんに提供できるよう、迅速に進めることができると考えています」。
有効性
以下の図1は、mOSのカプラン・マイヤー推定値(10.1カ月 vs 7.2カ月、HR=0.63、log-rank p=0.01)を示しており、死亡リスクが37%減少していることから、エルラグルシブ/GnP併用療法群とGnP単独療法群との比較において、エルラグルシブ/GnP併用療法群で治療を受けた患者に明らかな臨床的生存ベネフィットがあることを示している。
図1:Actuate-1801 Part 3B:2025年3月27日時点のmOSのカプランマイヤー推定値(トップラインデータカットオフ)。
mOSおよび1年生存率の改善に加えて、18ヵ月後および24ヵ月後においても生存の継続的なベネフィットが観察された(生存率はそれぞれ、エルラグルシブ/GnP併用群対GnP群で19.7%対4.4%、13.8%対0%)。
また、エルラグルシブ/GnP併用療法では、全奏効率が数値的に改善し(エルラグルシブ/GnP併用療法群29.0%対GnP併用療法群21.8%)、無増悪生存期間中央値および奏効期間中央値は、それぞれエルラグルシブ/GnP併用療法群5.6カ月対5.1カ月、エルラグルシブ/GnP併用療法群5.5カ月対GnP併用療法群4.0カ月と改善した。
安全性およびバイオマーカー所見
本試験は主要安全性エンドポイントも達成した。エルラグルシブ/GnP併用群における治療有害事象(TEAE)および重篤な有害事象(SAE)はGnP併用群で観察されたものと同様であり、エルラグルシブ/GnP併用群の良好なリスク・ベネフィット・プロファイルを示した。
治療関連有害事象(TRAE)はほとんどがグレード1~2であり、最も頻繁に観察されたTRAE(患者の約3分の2)は一過性の視覚障害で、可逆的かつ非進行性であった。
グレード3以上の好中球減少症が観察された一方で、発熱性好中球減少症および敗血症の発生率は両群で同程度であった。
投与前のサイトカイン解析では、CCL3、IL-1α、IL-18、TGF-β、TRAIL R3などの主要な免疫調節因子のベースライン値が低いことが示唆され、1年生存率の改善と相関していた。
CD8陽性およびグランザイムB陽性T細胞の増加、NK細胞の増加、および骨髄由来抑制細胞の減少が、エルラグルシブ治療患者の腫瘍生検でのみ観察された。この探索的な結果は、mPDAC患者においてエラグルシブが提唱する免疫調節作用の機序を裏付けるものである。
KOLイベント
アクチュエイト社は、本日2025年5月31日午後6時30分(米国東部標準時間)より、投資コミュニティー向けにKOLイベントを開催し、本データをレビューします。このウェビナーでは、アクチュエイトの社長兼最高経営責任者(CEO)ダニエル・シュミットが司会を務め、4人の著名なKOLが参加します:メイヨークリニック医科科学大学Tanios Bekaii-Saab医学博士(FACP)、ノースウェスタン大学ファインバーグ医学部Devalingam Mahalingam医学博士、アリゾナ大学がんセンターRachna Shroff医学博士、アリゾナ大学がんセンターMS、FASCO、マサチューセッツ総合病院Colin Weekes医学博士。
イベントの詳細
日時:2025年5月31日(土)午後6時30分(米国東部標準時
形式 対面およびライブ・ウェブキャスト
登録: こちらをクリック
当日の模様は、アクチュエイトのウェブサイトの投資家向け情報セクションでご覧いただけます。
Actuate-1801 Part 3B Studyについて
Actuate-1801 Part 3B試験(NCT03678883)は、mPDACの一次治療におけるエルラグルシブとGnPの併用療法とGnP単独療法の無作為化比較第2相試験です。本試験には、転移性疾患に対する全身治療歴のないmPDAC患者286人が登録され、エルラグルシブ治療群(エルラグルシブ+GnP)と対照群(GnP単独)に2:1で無作為に割り付けられた。エルラグルシブは9.3mg/kgの用量で、28日サイクルの各週の1日目に点滴静注される。本試験の主要評価項目は全生存期間中央値であり、OSは本試験全体を通して1年生存期間の推定値で要約される。副次評価項目はDCR、ORR、PFS、AEである。
GSK-3βの阻害は、化学療法活性の増強、自然抗腫瘍免疫の活性化、遺伝子発現の調節、腫瘍代謝の変化や上皮間葉転換(EMT)をもたらすなど、いくつかの相補的な機序によって腫瘍の増殖を抑制し、生存率を改善する可能性がある。
アクチュエイト・セラピューティクス社について
アクチュエイト社は、影響が大きく治療が困難な癌の治療法の開発に重点を置く臨床段階のバイオ医薬品企業である。アクチュエイト社の主要な治験薬であるエルラグルシブ(新規GSK-3β阻害剤)は、活性化B細胞のκ-光鎖-エンハンサー核因子(NF-kB)およびDNA損傷応答(DDR)を阻害することにより、腫瘍の成長を促進し、化学療法などの従来の抗癌剤に対する抵抗性に関与する癌の分子経路を標的とする。エラグルシブはまた、複数の免疫チェックポイントと免疫細胞の機能を制御することにより、抗腫瘍免疫を仲介する可能性がある。追加情報については、当社ウェブサイトhttp://www.actuatetherapeutics.com。
将来の見通しに関する記述
本プレスリリースには、当社およびその他の関係者の臨床試験および開発計画、ならびに当社業界に関する将来の見通しに関する記述が含まれています。予想する」、「信じる」、「継続する」、「可能性がある」、「推定する」、「期待する」、「意図する」、「可能性がある」、「かもしれない」、「進行中である」、「計画する」、「可能性がある」、「予測する」、「プロジェクトする」、「はずである」、「目標する」、「する予定である」、「だろう」、またはこれらの用語の否定形、あるいはその他の同等の用語は、将来見通しに関する記述を識別することを意図していますが、すべての将来見通しに関する記述がこれらの識別語を含んでいるわけではありません。本プレスリリースに含まれる、現在の事実もしくは現在の状況または過去の事実に関連する記述を除くすべての記述は、将来の見通しに関する記述です。従って、これらの記述には見積もり、仮定、重大なリスクおよび不確実性が含まれており、実際の結果が記述に示されたものと大きく異なる可能性があります。予備的データおよび未発表データは、より多くのデータが入手可能になった後、またはデータをより包括的に検討した後に変更され、さらに解釈される可能性があり、最終的な分析として依拠すべきではありません;臨床試験データが、規制当局や医学界で異なる解釈や評価の対象となるリスク、臨床および前臨床の医薬品開発には、タイムラインや結果が不確実な、長期的で費用のかかるプロセスが含まれること、先行する前臨床試験や初期の臨床試験の結果は必ずしも将来の結果を予測するものではなく、エラグルシブが良好な臨床結果や良好な前臨床試験結果を達成できない可能性があること、また、規制当局への申請や承認取得を適時に行うことができない可能性があること;FDAまたはEMAとの対話およびそのような機関が課す可能性のある開発基準を含め、さらなる患者の追加登録に成功しない、またはさらなる開発計画を確立または前進させることができない可能性があること、エラグルシブに副作用、有害事象、その他の特性または安全性リスクが伴う可能性があり、その結果、規制当局の承認が遅延または妨げられる可能性があること、臨床試験を中断または中止させる可能性があること、その他の否定的な結果をもたらす可能性があること、非臨床試験および臨床試験を実施するために第三者に依存していること、第三者のライセンサーに依存していること、および当社の知的財産権を維持し保護する能力があること;当社が他のバイオテクノロジー企業や製薬企業との大きな競争に直面していること、当社の財務状況により継続企業の前提に重要な疑義が生じ、2025年度第2四半期以降の事業資金を調達するために追加資本を必要としていることを含め、当社の開発活動資金調達能力、この必要な資本を短期間に許容可能な条件で、または全く調達できない場合、当社は開発プログラム、商業化努力またはその他の事業の遅延、制限、縮小または終了を余儀なくされる可能性があります。さらに、将来の見通しに関する記述は、「項目1A.2025年3月13日にSECに提出された2024年12月31日終了年度の年次報告書(フォーム10-K)、2025年5月15日にSECに提出された2025年3月31日終了四半期の四半期報告書(フォーム10-Q)、およびSECへのその他の提出書類に記載されている「リスク要因」の見出しを参照することにより、将来の見通しに関する記述の全体が制限されます。上記のリスク要因により、実際の結果や業績が、当社または当社のために作成された将来見通しに関する記述で表明されたものと大きく異なる可能性があるため、将来見通しに関する記述を過度に信頼すべきではありません。さらに、いかなる将来予想に関する記述も、それが作成された時点のものでしかありません。新たな要因は随時発生するものであり、どの要因が発生するかを予測することは不可能です。加えて、各要因が当社の事業に与える影響や、各要因または各要因の組み合わせによって実際の結果が将来の見通しに関する記述に含まれるものとどの程度異なるかを評価することはできません。法的に義務付けられている場合を除き、当社は、本プレスリリースの日付以降の事象や状況を反映したり、予期せぬ事象の発生を反映したりするために、そのような将来見通しに関する記述の修正を公表する義務を負うものではありません。
投資家連絡先
マイク・モイヤー
マネージング・ディレクター
ライフサイ・アドバイザーズLLC
mmoyer@lifesciadvisors.com
この発表に添付された写真は https://www.globenewswire.com/NewsRoom/AttachmentNg/ec493cba-bb28-4bc9-adae-263985865ae6 でご覧いただけます。